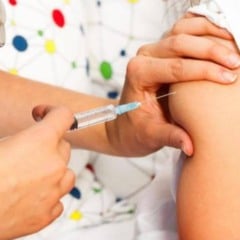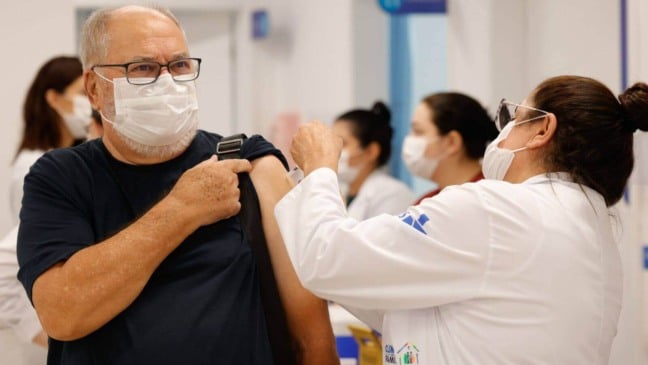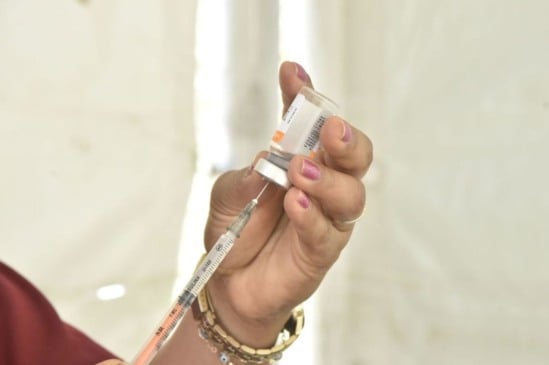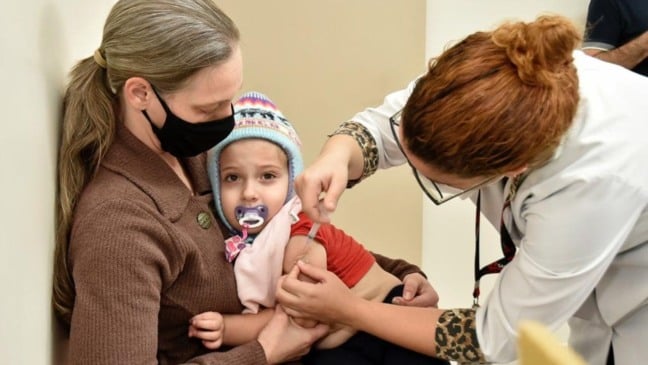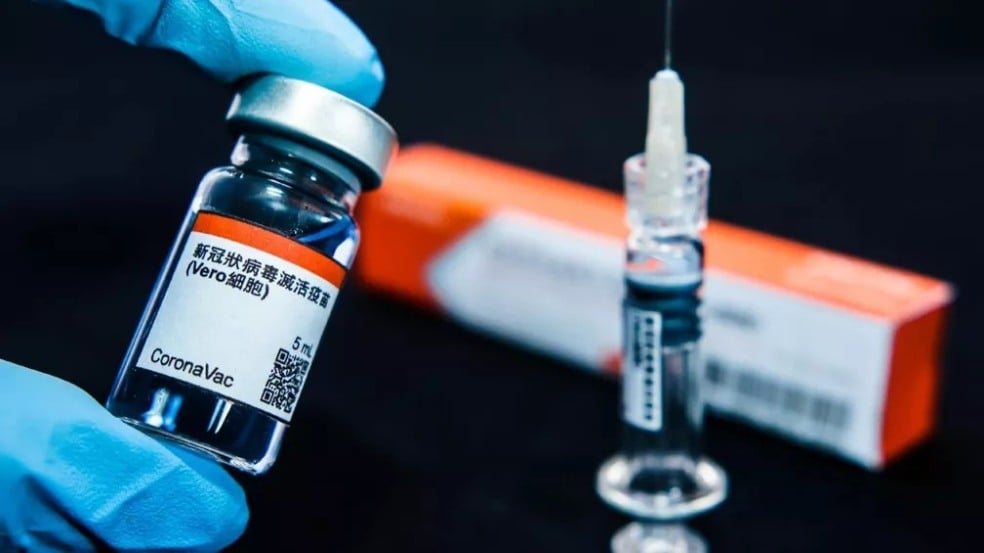
Nesta segunda-feira (21), a Agência Nacional de Vigilância Sanitária (Anvisa) certificou a farmacêutica chinesa Sinovac por Boas Práticas de Fabricação.
A equipe da Anvisa junto de observadores do Instituto Butantan que viajaram para a China concluíram a etapa após inspeção da produção da vacina CoronaVac, contra a Covid-19.
A inspeção e outras reuniões com executivos da empresa aconteceram entre os dias 30 de novembro e 4 dezembro. De acordo com uma nota publicada no Diário Oficial, o plano de ação do Instituto Butantan foi enviado para a Anvisa na quarta-feira (16). Enquanto isso, a conclusão da equipe técnica foi encerrada no domingo (20).
A autorização foi publicada 10 dias antes da previsão inicial que foi definida pela agência. A certificação é válida por dois anos e é um pré-requisito para o processo de registro da vacina no Brasil. Além disso, também é necessário para um eventual pedido de autorização de uso emergencial do imunizante no país.
Fase de testes
No mesmo dia da certificação, o Instituto Butantan anunciou que a terceira e última fase de testes clínicos da CoronaVac foi concluída.
Através das redes sociais, o instituto paulista também anunciou que “os resultados [da fase 3] serão encaminhados para a Agência Nacional de Vigilância Sanitária (Anvisa)”. Também afirmaram que a primeira vacina brasileira contra a Covid-19 estará pronta “em breve”.
É previsto que os resultados da fase 3 sejam divulgados nesta quarta-feira (23).