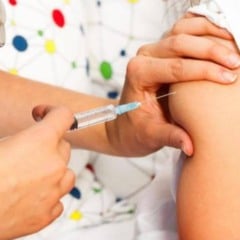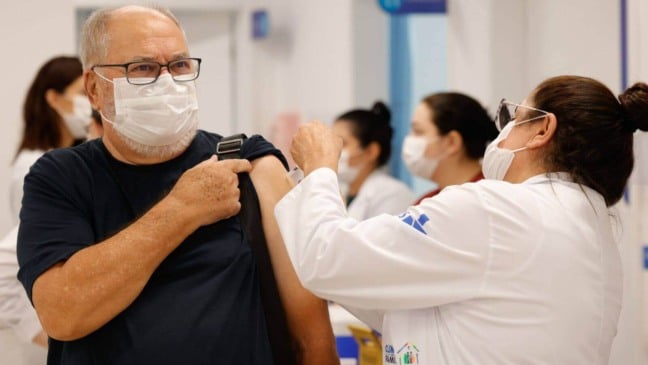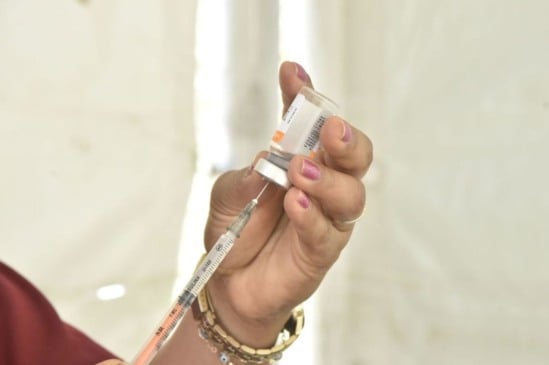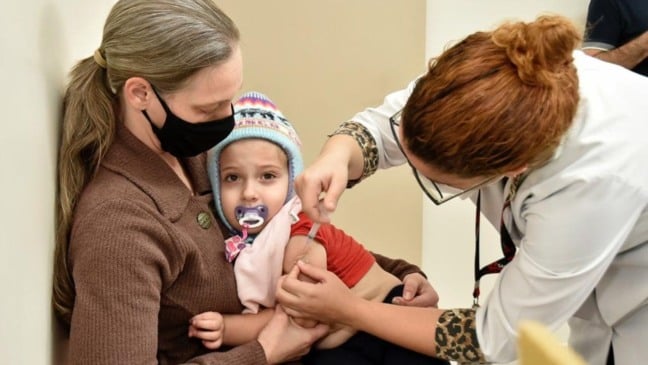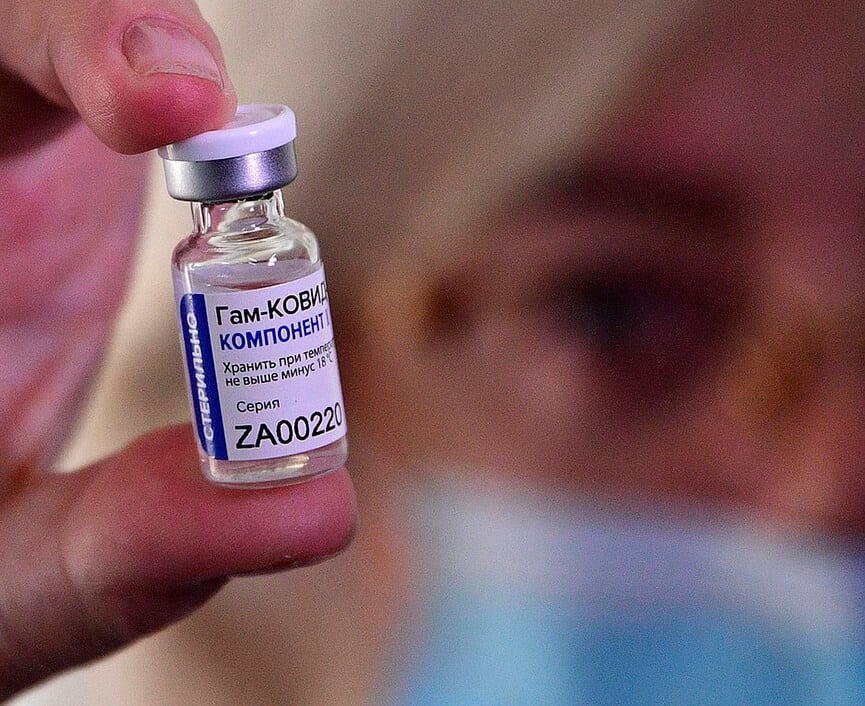
A Agência Nacional de Vigilância Sanitária (Anvisa) irá alterar nesta quarta-feira (3) o texto do guia que estabelece requisitos mínimos para o pedido de uso emergencial de vacinas para Covid-19, retirando a exigência de realização de estudo em fase 3 no Brasil.
A medida afeta diretamente a liberação provisória da vacina russa Sputnik V, favorita pelo governo da Bahia. A União Química, responsável pela produção do imunizante no país, não conseguiu a autorização para realizar o estudo com a vacina no país, no entanto, ele já teria sido realizado em outros países.
Além da vacina Sputnik V, a liberação também pode ajudar a vacina Covaxin, da farmacêutica indiana Bharat. Com o novo posicionamento da Anvisa, a estratégia regulatória para a aprovação do imunizante poderá ser otimizada.
Com informações das Agências.